エネファーム(家庭用燃料電池)の仕組み
①発電原理
水の電気分解の逆。それが燃料電池の原理
燃料電池は、「電池」と呼ばれていますが、“発電装置”と言った方がふさわしいものです。乾電池と違うのは、使い捨てではないという点です。水素(H₂)と酸素(O₂)があれば電気を作り続けます。
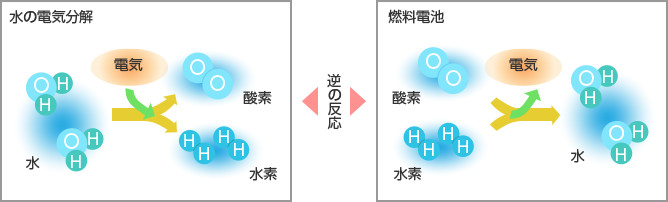
燃料電池は、「水の電気分解」と逆の原理で発電します。水の電気分解は、水に外部から電気を通して水素と酸素に分解します。燃料電池はその逆で、水素と酸素を電気化学反応させて電気を作ります。
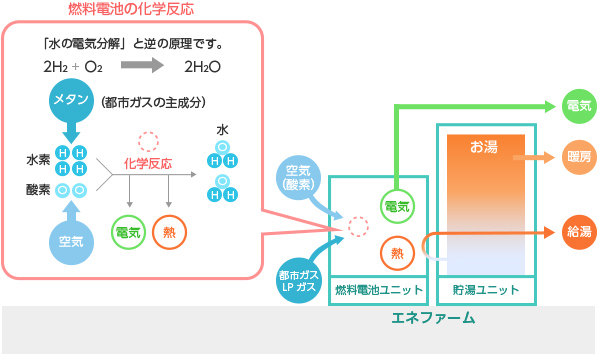
・酸素(O₂)は、空気中にあるものを利用します。
・水素(H₂)は、都市ガスの原料である天然ガスなどから取り出します。
②燃料電池の仕組み
燃料電池本体は「セルスタック」といいます
燃料電池本体をのぞいてみると、板のようなものがたくさん積み重なっています。これを「セル」といいます。
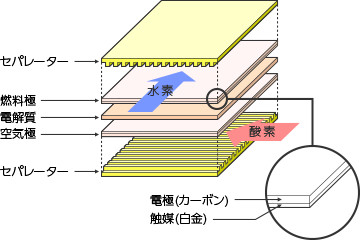
・ひとつのセルが作れる電気は、電圧約0.7V(ボルト)です。そこで、大きな電気を作るために、セルを積み重ねます。乾電池を直列につなぐのと同じことです。燃料電池本体は、セルが積み重なってできていることから、「セルスタック」と呼ばれます。
・たとえば1kW(キロワット)の電気を作るには、50枚ぐらいのセルを積み重ねます。
・セルとセルの間には「セパレーター」があります。となりどおしになる水素と酸素の通路を仕切り、さらに電気的につなぐ役割をしています。
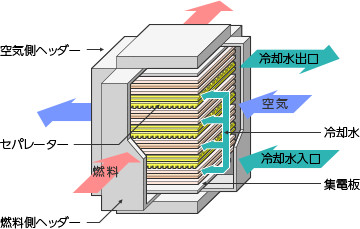
セル
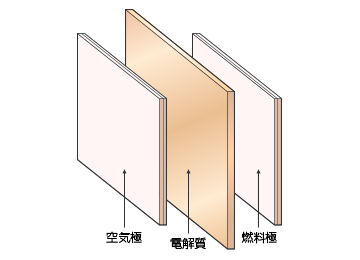
・セルは、燃料電池を作る単位となり、単電池とも呼ばれています。
・セルは、サンドイッチのような構造をしています。プラスの電極(=空気極)と、マイナスの電極(=燃料極)が、電解質をはさんでいます。乾電池が平らになったイメージです。
ポイントは、ココ!
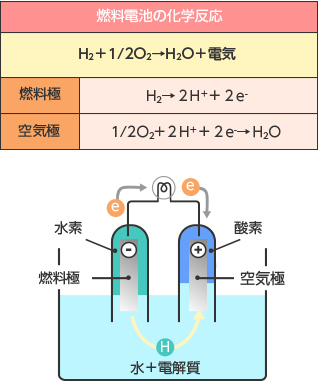
<PEFCの場合>
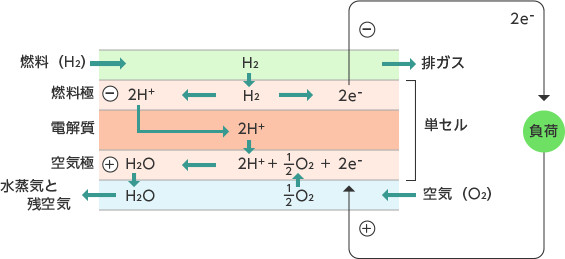
・空気極と燃料極は気体を通す構造をしていて、反応に必要な酸素や水素がその中を通ります。
・水素は電極中の触媒の働きで、電子を切り離して水素イオンになります。電解質はイオンしか通さないという性質を持っているため、切り離された電子は外に出て行きます。
・電解質の中を移動した水素イオンは、反対側の電極に送られた酸素と、外部から電線(外部回路)を通じて戻ってきた電子と反応して、水になります。
・この、「反応に関与する電子が外部回路を通ること」が原理の重要なポイントです。電子が電線を移動するということは、電流が流れるということ、つまり電気が発生するということなのです。
ポイントは、ココ!
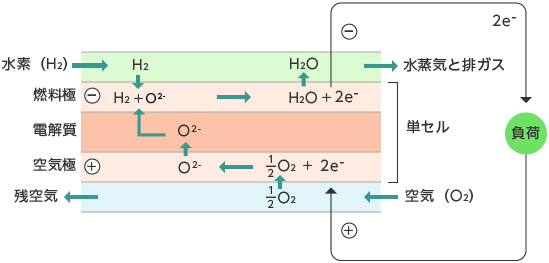
<SOFCの場合>
・空気極と燃料極は気体を通す構造をしていて、反応に必要な酸素や水素がその中を通ります。
・酸素は電極中の触媒の働きで、電子と反応して酸素イオンになります。電解質はイオンのみを通すという性質を持っているため、酸素イオンは電解質の中を移動します。
・電解質の中を移動した酸素イオンは、反対側の電極で電子を切り離して水素と反応し、水になります。切り離された電子は外部から電線(外部回路)を通じて空気極に戻ります。
・この、「反応に関与する電子が外部回路を通ること」が原理の重要なポイントです。電子が電線を移動するということは、電流が流れるということ、つまり電気が発生するということなのです。